ОПРЕДЕЛЕНИЕ ФИТОТОКСИЧНОСТИ СИМБИОТИЧЕСКИХ БАКТЕРИЙ (XENORHABDUS BOVIENII) ЭНТОМОПАТОГЕННЫХ НЕМАТОД НА НАЧАЛЬНЫХ ЭТАПАХ РАЗВИТИЯ SOLANUM LYCOPERSICUM MILL.
ОПРЕДЕЛЕНИЕ ФИТОТОКСИЧНОСТИ СИМБИОТИЧЕСКИХ БАКТЕРИЙ (XENORHABDUS BOVIENII) ЭНТОМОПАТОГЕННЫХ НЕМАТОД НА НАЧАЛЬНЫХ ЭТАПАХ РАЗВИТИЯ SOLANUM LYCOPERSICUM MILL.
Аннотация
В статье приведена оценка фитотоксичности продуктов метаболизма симбиотических бактерий Xenorhabdus nematophilus – симбионтов нематод вида Steinernema carpocapsae, а также X. bovienii – симбионта нематод S. feltiae и S. feltiae protense по показателям прорастания семян томата сорта Новичок (всхожесть) и интенсивности начального роста семян (длина побегов и корней, фитомасса корней). Предпосевная обработка семян томата продуктами метаболизма симбиотических бактерий энтомопатогенных нематод с различным титром живых и автоклавированных культур 103, 105 и 107 КОЕ/мл. Исследованиями выявлено, что наибольшей фитотоксичностью обладает штамм S. сarpocapsae во всех концентрациях, подавляя начало прорастания семян при сравнении с контролем (обработка водой) на 20-63%, уменьшая длину корней на 14-92%. Ростостимулирующими свойствами обладают симбиотические бактерии энтомопатегенных нематод S. feltiae и S. feltiae protense, проявляя высокий уровень биологического воздействия при концентрации 105 КОЭ/мг.
1. Введение
Имеющиеся современные технологии возделывания сельскохозяйственных культур предусматривают обязательные приемы, обеспечивающие стимулирование растений на начальных этапах развития с целью получения более устойчивых к различным болезням и вредителям, например, обработки и протравливание семян, опрыскивание посевов пестицидами. Такие способы борьбы экологически небезопасны, поэтому требуется дальнейший поиск и создание менее токсичных аналогов средств защиты. Мировая тенденция сокращения доз внесения агрохимикатов определяет возрастание необходимости использования в растениеводстве новых, дополнительных источников минерального питания и биологических средств защиты растений
, , . Использование микроорганизмов, в том числе и энтомопатогенных нематод (ЭПН), в биологической борьбе с насекомыми-вредителями и болезнями повсеместно повысилось и приобретает особую значимость в современном сельскохозяйственном производстве. Энтомопатогенные нематоды семейств Steinernematidae и Heterorhabditidae и их симбиотические бактерии широко изучаются во всем мире. Виды рода Xenorhabdus spp. являются грамотрицательными энтомопатогенными бактериями, которые живут в симбиозе с нематодами рода Steinernema . После проникновения в тело насекомого нематоды выпускают в гемоцель хозяина бактерии, которые быстро размножаются и производят различные метаболиты, как в vivo так и в in vitro условиях, которые преодолевая иммунную систему насекомых, убивают одновременно подавляя рост различных грибковых и бактериальных симбионтов предотвращая гниение трупа насекомых, что способствуют развитию нематод нематодно-бактериального комплекса . Продукция вторичных метаболитов с антибиотическими свойствами является общей характеристикой энтомопатогенных бактерий Xenorhabdus spp. Эти метаболиты не только имеют разнообразную химическую структуру, но также обладают широким спектром биологической активности с медицинскими и сельскохозяйственными интересами, такими как антибиотики, противогрибковые и инсектицидные, нематоцидные и противоязвенные, противоопухолевые и противовирусные. Исследованиями доказано, что антибактериальная активность бесклеточных культур симбиотических бактерий не снижается после хранения их при комнатной температуре в течение 6 дней, но при 37оС антибиотики распадаются через 4-5 дней. Автоклавирование при 121°С в течение 10 мин не влияет на антибиотическую активность бесклеточных культур . Целью проводимых исследований было изучение фитотоксичности живых и автоклавированных культур симбиотических бактерий рода Xenorhabdus, энтомопатогенных нематод сем. Steinernematidae, на ранних стадиях развития растений при внесении этих патогенов в почву в качестве средства защиты растений от насекомых и возбудителей заболеваний.2. Методы и принципы исследования
Лабораторные исследования проводились на базе Всероссийского Института защиты растений (г. Пушкин). Виды и штаммы симбиотических бактерий, используемые в экспериментах, были получены путем заражения гусениц большой вощинной моли (Galleria mellonella) видами нематод S. carpocapsae, S. feltiae и S. feltiae protense. Трупы погибших от заражения нематодами насекомых поверхностно стерилизовали в 70% спирте в течение 2 мин. и помещали для сушки в ламинарный поток воздуха в течение 3 мин. Затем из ложноножки отдельной гусеницы стерильно отбирали каплю гемолимфы, которую переносили в чашку Петри на питательную среду NBTA и инкубировали при 26°C. После 72 часов отбирали чистые колонии симбиотических бактерий (зеленые) из колоний одинакового размера и морфологии. Идентификацию первичных форм симбиотических бактерий проводили по методу Акюрста
. В лабораторных опытах при оценке влияния симбиотических бактерий и продуктов их метаболизма на возбудителей заболеваний картофеля грибные патогены высевали в чашки Петри на среду Чапека и выращивали при 25 °C в течение 5–7 суток. В качестве контроля использовали среду NBTA без симбиотических бактерий. Все варианты опытов и контроля были заложены в 4-х кратной повторности.Культура: томат штамбовый среднеранний, сорт Новичок (Lycopersiconesculentumvar. validum) . Фитотоксичность проверяли в модельных опытах на семенах томата с использованием культуры бактерий вида X. nematophila – симбионта нематод S. carpocapsae и X. bovienii - симбионта нематод S. feltiae, X. bovienii – симбионта нематод S .feltiae protense. Титр живых и автоклавированных культур имел три концентрации: 103 (1), 105 (2) и 107 (3) КОЕ/мг. Экспозиция замачивания - 2 часа. В опыте использовали 2 типа контроля: контроль 1 – сухие семена; контроль 2 – семена замачивали в стерильной воде на 2 часа. Обработанные семена проращивали на увлажненных ватных матрасиках (по 10 мл стерильной воды) в чашках Петри (рис. 1). Повторность опыта 3-кратная, по 10 семян на чашку. Через каждые двое суток добавляли по 1-2 мл воды для увлажнения матрасиков. Учет всхожести проводили на 7-е и 9-е сутки.
Рисунок 1 - Проращивание обработанных семян на увлажненных ватных матрасиках
3. Основные результаты и обсуждение
В лабораторных условиях нами изучено действие различных концентраций продуктов метаболизма трех изолятов симбиотических бактерий рода Xenorhabdus на ювенильной стадии развития семян томата. Установлено, что различные штаммы симбионтов ЭПН неоднозначно влияют на всхожесть семян томата (табл.1). Так, штамм симбиотических бактерий S. carpocapsae во всех концентрациях подавлял начало прорастания семян по сравнению с контрольным вариантом 2 (замачивание) на 30-57% на 7-е сутки и 20-63% на 9-е сутки. Наибольшая всхожесть на 7-9-й день была получена от применения автоклавированной культуры при концентрации 103 КОЭ/мг симбиотических бактерий S. Feltiae, на 27 % и 37% по сравнению с контролем 2 (замачивание), соответственно.
Таблица 1 - Показатели всхожести семян в зависимости от действия симбиотических бактерий рода Xenorhabdus spp
Энтомопатогенные нематоды | Время экс., сут. | Всхожесть, % | |||||||
Живая культура бактерий, титр (КОЭ/мг) | Автоклавированная культура бактерий, титр (КОЭ/мг) | контроль | |||||||
103 | 105 | 107 | 103 | 105 | 107 | Н2О | сухой | ||
S. carpocapsae | 7 | 27 | 27 | 10 | 3 | 10 | 30 | 60 | 27 |
9 | 40 | 50 | 23 | 7 | 17 | 43 | 70 | 33 | |
S. feltiae protense | 7 | 53 | 47 | 30 | 40 | 23 | 43 | 43 | 47 |
9 | 53 | 47 | 37 | 43 | 27 | 47 | 47 | 50 | |
S. feltiae | 7 | 50 | 53 | 23 | 70 | 33 | 47 | 43 | 47 |
9 | 53 | 60 | 37 | 80* | 37 | 53 | 47 | 50 | |
НСР095 | 2,08 | ||||||||
Исследования биометрических показателей с проведением сравнительной оценки фитотоксичности симбиотических бактерий первичных форм продуцентов Xenorhabdus, симбионтов различных видов ЭПН на растения показали достоверное увеличение длины стебля на 25% при обработке живой культурой S. feltiae protense в концентрации 105 КОЭ/мг. Применение автоклавированной культуры штамма S. feltiae в концентрации 103 и 107 КОЭ/мг также влияла на увеличение длины стебля на 37,5 и 12,5%, соответственно. Живые культуры всех исследуемых штаммов бактерий в концентрации 107 КОЭ/мг вызывали ингибирование роста стеблей (рис.2, а).
При применении штамма симбиотических бактерий S. carpocapsae в различных концентрациях как живой, так и автоклавированной культуры наблюдали ингибирование длины стебля, 16-68 % относительно второго контроля (обработка водой). Как видно из представленных данных в таблице 2, отмечено замедление процессов роста основного корня в обработанных штаммами вариантах и всеми концентрациями по сравнению с контролями вариантами. Только обработка живой культурой штамма S. feltiae protense в концентрации 105 способствовала росту корня на 26% по сравнению с первым контрольным вариантом (рис.2, б).
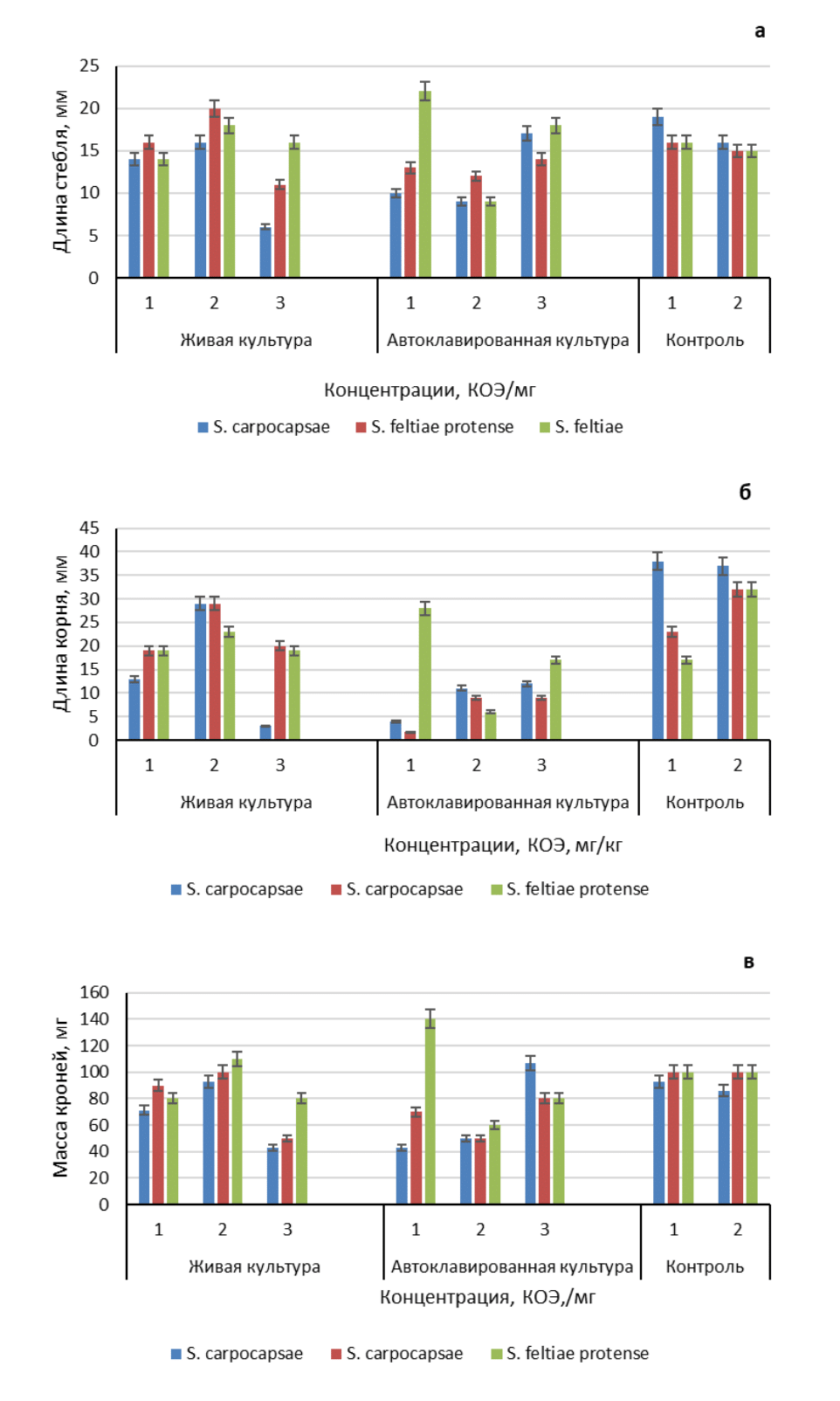
Рисунок 2 - Влияние штаммов симбиотических бактерий – симбионтов S. carpocapsae, S. feltiae protense, S. feltiae на биометрические показатели растений томата:
а - длина стебля, мм; б - длина корня, мм; в – масса корня, мг; концентрации: 1 – 103; 2 – 105; 3 – 107; контроль: 1 – сухой; 2 – обработка водой
4. Заключение
Таким образом, полученные данные свидетельствуют о том, фитотоксичность симбиотических бактерий Xenorhabdus bovienii энтомопатогенных нематод S. сarpocapsae, S. feltiae, S. feltiae protense. на начальных этапах развития томата зависит от штамма бактерии и его концентрации. Исследованиями выявлено, что живые штаммы симбиотических бактерий более фитотоксичны, чем автоклавированные. Наибольшей фитотоксичностью обладает штамм S. сarpocapsae. Симбиотические бактерии энтомопатегенных нематод S. feltiae и S. feltiae protense обладают хорошо выраженным ростостимулирующим свойством и проявляют высокий уровень биологического воздействия при концентрации 105 КОЭ/мг.
Полученные результаты подчеркивают значительный потенциал симбиотических бактерий Xenorhabdus bovienii энтомопатогенных нематод S. сarpocapsae, S.feltiae, S.feltiae в качестве полифункционального биологического средства для увеличения всхожести, влияния на ростовые процессы. Они дают практическую информацию для их применения в качестве средств повышения устойчивости и защиты сельскохозяйственных культур от вредителей и болезней.
